2020-02-17
栾杰
DOI:10.3760/cma.j.issn.1009-4598.2017.s1.000
基金项目:卫生部临床重点学科项目,首都特色医疗项目(两项)、首都卫生发展科研专项、国家卫计委公益性行业研究专项
作者单位:100144北京,中国医学科学院整形外科医院乳房整形美容中心
通信作者:栾杰,Email:doctorluan@vip.163.com
乳房再造是整形外科一个极富创造性和挑战性的领域。近年来,随着我国乳腺癌发病率的不断增高,乳腺癌切除后的乳房再造成为主要的患者群。相比20年前,虽然乳腺癌切除手术的范围在不断缩小,但局部条件不足与供区缺乏仍是乳房再造面临的巨大挑战;再造手术的组织创伤和功能破坏仍然很大,对许多乳腺癌患者而言是又一次难以承受的打击,以上成为了制约乳房再造国内推广的主要障碍。同时,患者对再造乳房形态的期望以及对手术安全性的要求日益增高,如何减少患者的再次手术创伤,减少甚至避免产生新的瘢痕,对整形外科技术的创新提出了更高的要求。我们认为:减少乳房再造对患者的二次创伤,让患者付出更少、得到更多,是当今乳房再造技术发展的趋势和方向。为此,我们提出了“乳房再造精细化、微创化和个性化”的理念和技术,旨在创造供、受区条件、减少组织和功能损伤、减少和避免产生新的瘢痕、提高再造手术效果,并围绕这一目标进行了一系列技术创新和改进。本文简要总结了我院近10年来在精细化与微创化理念指导下,对乳房再造技术的创新与改进工作。
一、 血管重构腹壁下动脉穿支皮瓣(DIEP)乳房再造
DIEP皮瓣可提供的组织量大,降低了供区损伤,是目前最常用于乳房再造的显微外科皮瓣。然而,单侧DIEP血管蒂无法保证两侧腹部皮瓣的血供,而双侧DIEP不仅增加了手术时间,更加大了对腹直肌结构和功能的破坏。有学者指出,应常规去除 DIEP皮瓣远端容易发生血运不良的区域。但是,当腹部供区组织量不足或者需要再造的乳房缺损较大时,DIEP皮瓣远端的组织量则尤为重要。如何在改善皮瓣血供的同时,尽可能减少对腹部结构的破坏一直是该手术技术创新努力的方向。
2009年,我们在国内首先报道了腹壁浅静脉(SIEV)皮瓣乳房再造[1],在获取同样腹部皮瓣的同时,避免了对腹直肌及前鞘的破坏。但由于SIEV的变异太大,影响了其普及应用。有研究发现,当DIEP皮瓣静脉回流发生阻塞时,通过SIEV回流通路可以解决术后皮瓣静脉危象的问题。我们在临床上发现,通过SIEV增加静脉回流可以改善DIEP皮瓣远端的血供,并用小型猪建立了不同静脉增流模式DIEP皮瓣的动物模型,通过动物实验及临床试验对皮瓣深、浅静脉增流效果的血流动力学情况进行了观察和评价,证实通过增加DIEP皮瓣的静脉回流通路,可以有效地扩大皮瓣的血流灌注范围[2-4]。随后,应用SIEV进行静脉增流的模式相继被提出,包括将DIEV和SIEV分别与胸廓内和胸背血管相吻合,也有学者尝试将对侧SIEV与胸廓内静脉的穿支进行吻合。2012年,我们创立了一种更为简便有效的静脉增流模式,即直接将双侧腹壁浅静脉对接,形成了一个全新的“双侧SIEV搭桥静脉增流的DIEP皮瓣”[5-6]。这种对皮瓣内血管进行重构的精细化技术减少了对腹直肌的破坏,显著改善了皮瓣的血液供应,扩大了DIEP皮瓣远端的成活面积,成功实现用一侧DIEP血管蒂携带了全部皮瓣进行乳房再造(图1),达到在获取更多组织的同时减少损伤的目的。
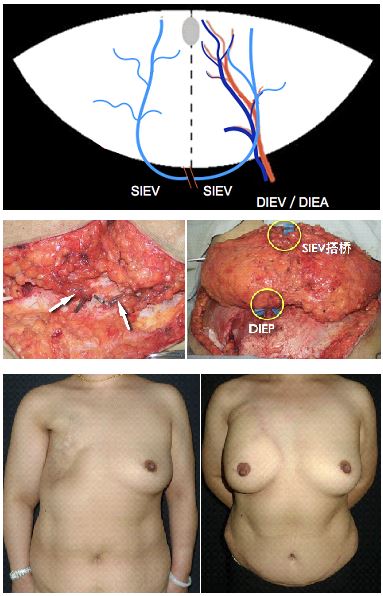
图1 双侧SIEV搭桥静脉增流DIEP皮瓣乳房再造 A:双侧SIEV分离完成待吻合;B:双侧SIEV吻合成功,皮瓣仅携带1支DIEP血管;C:术前;D:全部再造过程完成后1年(图1 宽:8cm 高:11.97cm)
二、 经单一腋下切口内窥镜辅助背阔肌肌瓣乳房再造
背阔肌肌瓣转移是一种常用的自体组织再造乳房方法,可以单独或与假体联合进行全乳房再造。传统方法除了使用腋下切口或前胸壁切口之外,还需要在背部增加1条超过10cm长的切口切取背阔肌肌瓣。其代价是在背部遗留1条十分明显的手术瘢痕,破坏了背部的美观,常常成为患者无法接受这一术式的原因。
曾有医生尝试将内窥镜技术用于背阔肌肌瓣的剥离,却因无法克服背部生理弯曲对操作的阻碍,难以通过单一腋窝切口获取全部的背阔肌。即使应用达芬奇手术机器人,也需要在侧胸部做三个切口,无法达到背部无瘢痕的美观效果。我们借鉴在内窥镜隆乳术中积累的大量经验,重新设计了适合背部生理弯曲,能使视野充分暴露的内窥镜辅助拉钩,采用我们首创的分体式内窥镜操作技术,大大降低了内窥镜下剥离背阔肌的操作难度,打破了常规内窥镜操作方法难以突破的技术瓶颈,仅通过1个腋窝隐蔽切口实现了完整背阔肌肌瓣的切取及乳房再造,背部不留任何切口痕迹,在减少损伤的同时,实现了微创化的美观效果(图2)。
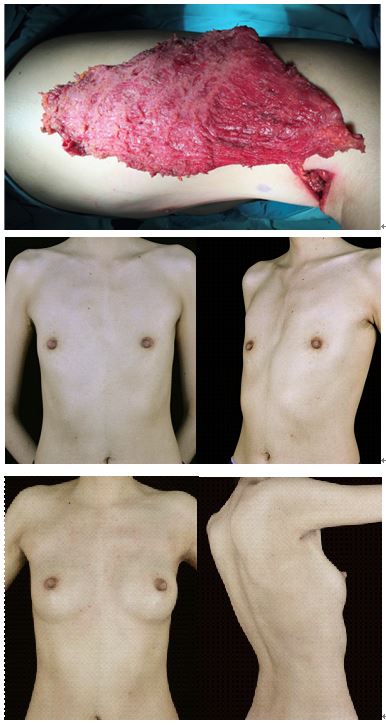
图2 内窥镜辅助经单一腋窝切口背阔肌肌瓣复合假体乳房再造术 A:内窥镜辅助经单一腋窝切口切取的背阔肌肌瓣,仅保留血管蒂与身体相连,经同1切口彩内窥镜技术分离前胸壁皮下腔隙,置入假体和肌瓣;B、C:术前正位、左斜位,显示严重胸廓畸形;D、E:术后半年正位、右后斜位,显示背部和胸前均未有手术切口(图2 宽:8cm 高:14.76cm)
三、组织外扩张联合水动力技术自体脂肪移植乳房再造
采用自体脂肪移植进行乳房再造损伤小、恢复快,对于胸部术区皮肤条件良好、身体其他部位有多余脂肪、健侧乳房体积不大的患者,无疑是最佳选择。然而,乳腺癌切除造成的乳房缺损情况较为复杂,多数都存在瘢痕粘连、局部组织过薄、皮肤放疗损伤等不利条件,术后极易出现脂肪液化吸收、坏死、结节、囊肿等并发症,最终导致乳房再造手术失败。基于以上原因,过去的观点认为自体脂肪移植只能作为乳房再造手术中增加假体表面组织覆盖厚度、调整乳房对称性的辅助手段。
组织外扩张技术辅助自体脂肪移植是由美国医生Roger发明的一项新技术。组织外扩张技术能够明显改善乳腺癌切除后的受区条件,提高脂肪移植存活率,使单纯应用脂肪移植的全乳房再造由不可能变为了可能。我们在国内率先开展应用脂肪移植技术进行乳房再造并取得成功[7-8]。此后进一步将组织外扩张技术与水动力脂肪采集技术相结合,为自体脂肪移植乳房再造创造最佳条件。其最大的优点是既不增加胸部切口瘢痕,也没有供区瘢痕,不损伤功能,且对于较肥胖的患者来说,乳房再造的同时又进行了减脂塑身,最大程度地实现了乳房再造的微创化(图3)。同时,我们还开展了一系列基础和临床研究,证明水动力技术能够更好地保持脂肪细胞的活力[9-10]。通过术后三维体积测量、核磁检查及B超检查,评估脂肪移植乳房再造的效果及并发症发生率,证实了联合应用组织外扩张技术和水动力脂肪采集技术的合理性和科学性。
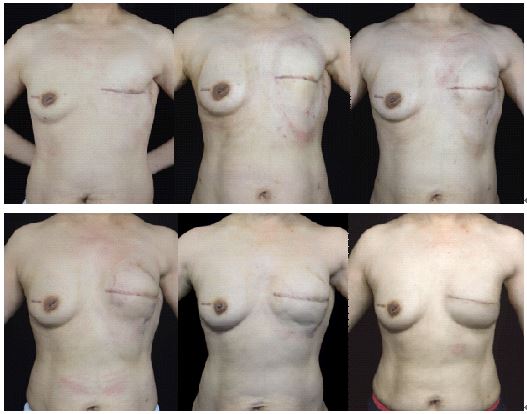
图3 BRAVA组织外扩张联合水动力技术自体脂肪移植乳房再造术,患者经历了四次脂肪移植和下皱襞成形术A:术前; B:第1次脂肪移植术后3个月; C:第2次脂肪移植术后3个月;D:第3次脂肪移植术后3个月;E:第4次脂肪移植术后3个月;F:下皱襞成形术后6个月(图3 宽:11cm 高:8.46cm)
四、血管影像技术和荧光显像技术在游离皮瓣乳房再造中的应用
对于应用显微外科的自体组织游离皮瓣移植技术来说,术前明确供、受区血管及穿支的位置、走向、粗细等情况,对于确定手术方案、缩短手术时间具有非常实际的意义。我们在国内首先将CTA技术应用于DIEP皮瓣的术前血管探查,可以三维显示和评估供受区的血管条件(图4),在术前对皮瓣血管重构的方案进行设计,大大方便了手术,节省了术中探查时间,降低了风险[11-13]。另外,我们在国内最早应用荧光显像技术(ICG)对DIEP皮瓣进行术中探测,近年来又引进了国际最先进的SPY荧光显像设备,可以更加直观地观察皮瓣的血供范围,为评估皮瓣成活区域提供参考指标,从而提高了对皮瓣成活范围的判断。
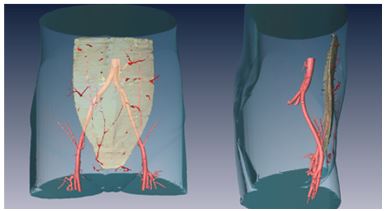
图4 基于CTA数据三维重建技术显示的DIEA以及经腹直肌前鞘穿出的DIEP(图4 宽:8cm 高:4.37cm)
五、数字化技术
自2005年起,我们应用三维数字化扫描技术对每一例乳房整形患者进行术前、术后扫描,建立了国内最早、最大的乳房整形手术三维数据库,形成了一套精确测量乳房对称性与体积的方法[14-16]。利用三维数据进行乳房美学评价、手术三维设计和长期追踪,可对脂肪移植乳房再造的体积保持率进行连续追踪和精确测量(图5),并可结合BREASTQ量表对不同术式再造术后的效果进行评价,从而使乳房再造的精细化有了客观、量化的工具[17-19]。
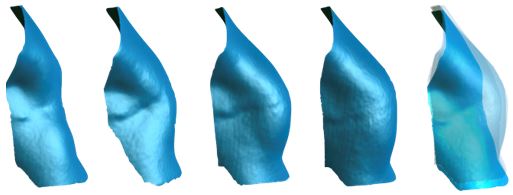
图5 应用三维光学扫描技术,对脂肪移植乳房再造术后乳房体积的变化进行连续追踪和精确观测(图5 宽:11cm 高:4.17cm)
综上所述,我们确立了“精细化、微创化和个性化”的乳房再造理念,在乳房再造领域不断创新、不断发展,使患者获益最大化的同时,不断追求实现损伤最小化。相信“精细化、微创化和个性化”也将必然成为乳房再造的发展趋势。
参考文献
[1] 栾杰,穆大力,穆兰花,等.应用SIEA皮瓣行乳房再造——附3例报告[J].中国美容医学,2009,18(02):143-144. DOI:10.3969/j.issn.1008-6455.2009.02.002.
[2] Minqiang X, Jie L, Lanhua M,et al.A new experimental venous super-drained transmidline abdominal skin flap model in pig[J]. J Plast Reconstr Aesthet Surg. 2010,63(10):764-5.DOI: 10.1016/j.bjps.2010.04.046.
[3] Minqiang X, Jie L, Dali M,et al.Transmidline abdominal skin flap model in pig: refinements and advancements[J]. J Reconstr Microsurg. 2012,28(2):111-118.DOI: 10.1055/s-0031-1289162. Epub 2011 Oct 13.
[4] Minqiang X, Jie L, Dali M, et al.Hemodynamic effect of different kinds of venous augmentation in a pig transmidline flap model of DIEP flap[J]. J Reconstr Microsurg. 2013,29(6):379-386.DOI: 10.1055/s-0033-1343497. Epub 2013 May 13.
[5] Xin Q, Luan J, Mu H, et al. Augmentation of venous drainage in deep inferior epigastric perforator flap breast reconstruction: efficacy and advancement[J]. J Reconstr Microsurg. 2012,28(5):313-318.DOI: 10.1055/s-0032-1311688. Epub 2012 Apr 19.
[6] 辛敏强,栾杰,穆大力.静脉增流DIEP皮瓣的临床应用及效果评价[J].中国美容医学,2015,(10):1-4.
[7] 穆大力,栾杰,穆兰花,等.自体脂肪颗粒注射移植在乳房局部畸形矫正中的应用[J].中国美容整形外科杂志,2012,23(12):709-711.DOI: 10.3969/j.issn.1673-7040.2012.12.002.
[8] 穆大力,栾杰,郭小双.Brava辅助自体脂肪移植矫正乳房局部缺损[J].组织工程与重建外科杂志,2015,(02):78-79.DOI: 10.3969/j.issn.1673-0364.2015.02.007.
[9] Fu S, Luan J, Xin M, et al. Fate of adipose-derived stromal vascular fraction cells after co-implantation with fat grafts: evidence of cell survival and differentiation in ischemic adipose tissue[J]. Plast Reconstr Surg, 2013,132(2):363-373.DOI: 10.1097/PRS.0b013e31829588b3.
[10] Yin S, Luan J, Fu S ,et al. Does water-jet force make a difference in fat grafting? In vitro and in vivo evidence of improved lipoaspirate viability and fat graft survival[J]. Plast Reconstr Surg,2015,135(1):127-38.DOI: 10.1097/PRS.0000000000000780.
[11] Xin M, Luan J, Mu L, et al. The value of multidetector-row CT angiography for pre-operative planning of breast reconstruction with deep inferior epigastric arterial perforator flaps[J]. The British Journal of Radiology,2010, (83): 40–43. DOI: 10.1259/bjr/29140440. Epub 2009 Jul 6.
[12] Xin M, Luan J, Mu L,et al. The efficacy of preoperative vascular mapping by MDCTA in selecting flap in abdominal flap breast reconstruction[J]. Breast J,2011,17(2):138-142.DOI: 10.1111/j.1524-4741.2010.01048.x. Epub 2011 Feb 7.
[13] 辛敏强,栾杰,穆兰花.MDCTA指导下的腹部皮瓣乳房再造术式选择[J].中国美容医学,2009,18(12):1713-1717.DOI: 10.3969/j.issn.1008-6455.2009.12.001.
[14] 王凌宇,栾杰,李彦生,等.CT数据三维重建乳房体积测量方法的建立及人为影响因素分析[J].中华医学美学美容杂志,2010,16(02):77-80.DOI:10.3760/cma.j.issn.1671-0290.2010.02.002.
[15] Liu C, Luan J, Mu L,et al.The role of three-dimensional scanning technique in evaluation of breast asymmetry in breast augmentation: a 100-case study[J]. Plast Reconstr Surg,2010,126(6):2125-2132.DOI: 10.1097/PRS.0b013e3181f46ec6.
[16] 刘春军,吉恺,孙晶晶.乳房对称性的三维数字化分析[J].中华整形外科杂志,2013,29(05):353-356.DOI: 10.3760/cma.j.issn.1009-4598.2013.05.009.
[17] Liu C, Ji K, Sun J,et al. Does respiration influence breast volumetric change measurement with the three-dimensional scanning technique? [J]. Aesthetic Plast Surg,2014,38(1):115-119.DOI: 10.1007/s00266-013-0247-5. Epub 2013 Dec 13.
[18] Liu C, Luan J, Ji K,et al. Measuring volumetric change after augmentation mammaplasty using a three-dimensional scanning technique: an innovative method[J]. J Aesthetic Plast Surg, 2012, 36(5):1134-1139.DOI: 10.1007/s00266-012-9944-8. Epub 2012 Jul 26.
[19] 刘春军,栾杰.乳房再造与乳腺癌患者的生活质量[J].中华整形外科杂志,2015,31(02):155-157.DOI: 10.3760/cma.j.issn.1009-4598.2015.02.024.
(收稿日期:2017-06-19)